Bindungsenergien: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung |
|||
| Zeile 10: | Zeile 10: | ||
Da man die Massenbestimmung mit atomphysikalischen Meßmethoden | Da man die Massenbestimmung mit atomphysikalischen Meßmethoden | ||
({{FB|Massenspektrometer}}) durchführt, versteht man unter Mc² die Masse | ({{FB|Massenspektrometer}}) durchführt, versteht man unter Mc² die '''Masse | ||
des Atoms, d.h. man muß noch die Elektronenmassen abzüglich ihrer | des Atoms''', d.h. man muß noch die Elektronenmassen abzüglich ihrer | ||
Bindungsenergien berücksichtigen. Deshalb bezieht man die | Bindungsenergien berücksichtigen. Deshalb bezieht man die | ||
{{FB|Masseneinheit}} 1 <math>m_u</math> auf 1/12 der Masse des neutralen <math>C^{12}</math>-Atoms. | {{FB|Masseneinheit}} 1 <math>m_u</math> auf 1/12 der Masse des neutralen <math>C^{12}</math>-Atoms. | ||
:<math>m_uc^2 = 931,478MeV</math> | |||
<math> | {{AnMS|Oftmals wird die Wasserstoffmasse statt der Protonenmasse zur Berechnung der Binduungsenergie verwendet, da so die Elektronenmassen implizit berücksichtigt werden. | ||
:<math>B=(Z m_H+N m_m-m_A)c^2</math>{{Quelle|BS|Gl. 4.7}} }} | |||
==Massenspektrometrie== | |||
Prinzip der {{FB|Massenspektrometrie}}: Durch die Messung der '''Energie''' <math>E = | Prinzip der {{FB|Massenspektrometrie}}: Durch die Messung der '''Energie''' <math>E = | ||
\frac{1}{2}mv^2</math> und des '''Impulses''' <math>p = mv</math> wird die Masse <math> m = p^2/2E</math> bestimmt. | \frac{1}{2}mv^2</math> und des '''Impulses''' <math>p = mv</math> wird die Masse <math> m = p^2/2E</math> bestimmt. | ||
| Zeile 30: | Zeile 32: | ||
;magn. Feld: <math>\frac{mv^2}{r}=e v B \to p=mv=e r B</math> {{FB|Impulsmessung}} | ;magn. Feld: <math>\frac{mv^2}{r}=e v B \to p=mv=e r B</math> {{FB|Impulsmessung}} | ||
==Bindungsenergie pro Nukleon== | |||
Ergebnis für Bindungsenergie pro Nukleon B/A | Ergebnis für Bindungsenergie pro Nukleon B/A | ||
| Zeile 55: | Zeile 57: | ||
Ladung muss bekannt sein und ungleich 0 sein --> Neutronenmasse nicht bestimmbar (Umweg Deuteriumkern, Bindungsenergie) | Ladung muss bekannt sein und ungleich 0 sein --> Neutronenmasse nicht bestimmbar (Umweg Deuteriumkern, Bindungsenergie) | ||
===Prüngsfragen=== | |||
Version vom 17. August 2011, 13:01 Uhr

|
Der Artikel Bindungsenergien basiert auf der Vorlesungsmitschrift von Moritz Schubotz des 3.Kapitels (Abschnitt 0) der Kern- und Strahlungsphysikvorlesung von Prof. Dr. P. Zimmermann. |
Die Abfrage enthält eine leere Bedingung.
Da man die Massenbestimmung mit atomphysikalischen Meßmethoden
(Massenspektrometer) durchführt, versteht man unter Mc² die Masse
des Atoms, d.h. man muß noch die Elektronenmassen abzüglich ihrer
Bindungsenergien berücksichtigen. Deshalb bezieht man die
Masseneinheit 1 auf 1/12 der Masse des neutralen -Atoms.
| ANMERKUNG Schubotz: Oftmals wird die Wasserstoffmasse statt der Protonenmasse zur Berechnung der Binduungsenergie verwendet, da so die Elektronenmassen implizit berücksichtigt werden. |
Massenspektrometrie
Prinzip der Massenspektrometrie: Durch die Messung der Energie und des Impulses wird die Masse bestimmt.
Prinzipieller Aufbau eines Energie und Impulsfilters in einem Massenspektrographen durch elektrische bzw. magnetische Felder:
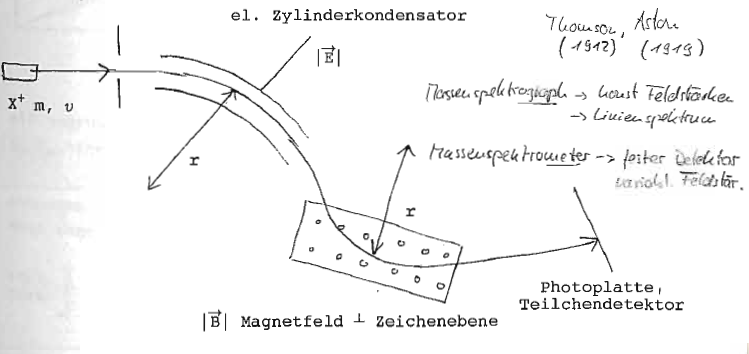
- el. Feld
- ·Energiemessung
- magn. Feld
- Impulsmessung
Bindungsenergie pro Nukleon
Ergebnis für Bindungsenergie pro Nukleon B/A

Im Mittel , d.h. ~ 1% der Ruhemasse •
Maximum bei ca. (Eisen), danach wegen wachsender Coulombabstoßung Abnahme um ca. 1 MeV auf bei . Größere Unregelmäßigkeiten bei leichten Kernen bis , besonders ausgeprägt bei:
- Deuterium
- Helium
Weitere Informationen
(gehört nicht zum Skript) nächstes Kapitel

merken
Idee: Zentripetalkraft = Lorentzkraft
merke Spektrograph erzeugt Bild
Auflösungsvermögen absoulute Massenbestimmung (bekannte Radien, E und B Felder, Ladung (5-Größen))
Ladung muss bekannt sein und ungleich 0 sein --> Neutronenmasse nicht bestimmbar (Umweg Deuteriumkern, Bindungsenergie)
Prüngsfragen
- ↑ Bergmann-Schaefer: Lehrbuch der Experimentalphysik, Band 4: Bestandteile der Materie. 2. Auflage 2003, ISBN 978-3-11-016800-6 Gl. 4.7



















